- Dãy chuyển động hóa học tập của sắt kẽm kim loại là dãy các kim nhiều loại được bố trí theo chiều sút dần mức độ chuyển động hóa học của chúng.
Bạn đang xem: Dãy hoạt động hóa học của kim loại: tính chất và cách để nhớ nhanh
- Dãy hoạt động vui chơi của một số kim loại:

* Mẹo nhớ: Khi (K) bà (Ba) con (Ca) nào (Na) may (Mg) áo (Al) liền kề (Zn) fe (Fe) lưu giữ (Ni) quý phái (Sn) phố (Pb) hỏi (H) cửa (Cu) sản phẩm (Hg) á (Ag) phi (Pt) âu (Au)
II. Ý nghĩa của dãy vận động hóa học của kim loại
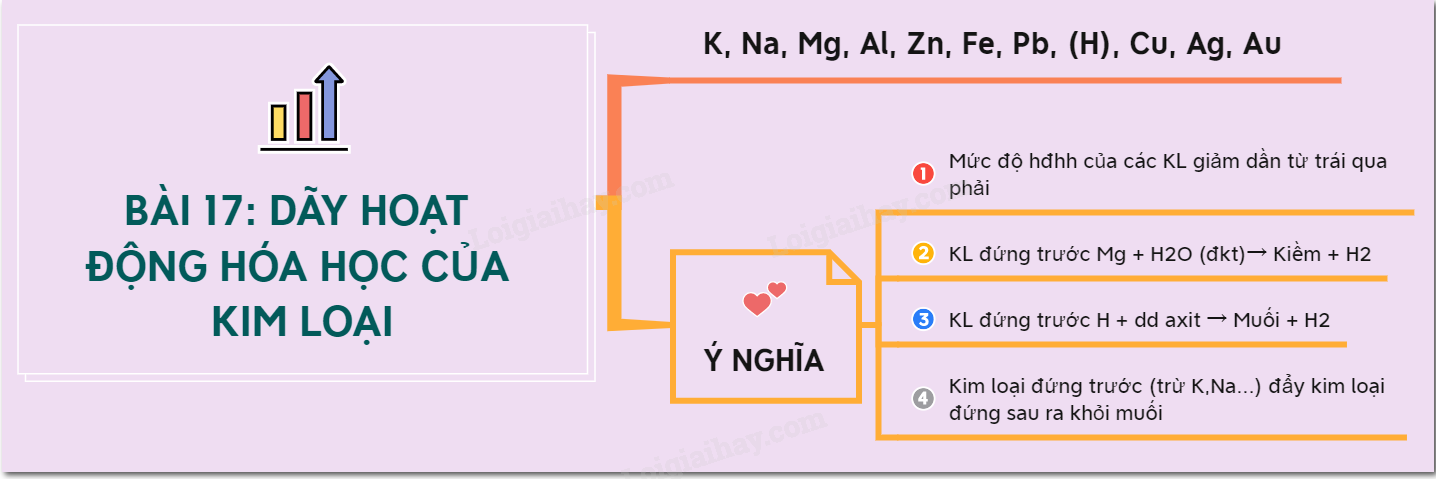
a) cường độ hóa học của những kim loại bớt dần từ bỏ trái quý phái phải
=> K là kim loại hoạt động mạnh nhất và Au là kim loại chuyển động kém nhất.
b) kim loại đứng trước Mg (K, Ba, Ca, Na) bội phản ứng được với nước ở nhiệt độ thường.
2Na + 2H2O → 2Na
OH + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
c) kim loại đứng trước H chức năng với hỗn hợp axit (HCl; H2SO4loãng,….) tạo ra H2
Fe + 2HCl → Fe
Cl2 + H2 ↑
Cu + 2HCl → không phản ứng (vì Cu che khuất H)
d) sắt kẽm kim loại không chảy trong nước (từ Mg quay trở lại sau) đẩy được sắt kẽm kim loại đứng sau nó ra khỏi dung dịch muối
Fe + Cu
SO4 → Fe
SO4 + Cu
Cu + 2Ag
NO3 → Cu(NO3)2 + 2Ag
Chú ý: Khi cho Na vào hỗn hợp Cu
Cl2 thì:
+ Na phản nghịch ứng với nước trước: 2Na + 2H2O → 2Na
OH + H2↑
+ sau đó xảy ra bội phản ứng: Cu
Cl2 + 2Na
OH → Cu(OH)2↓ + 2Na
Cl
Sơ đồ tứ duy: Dãy hoạt động hoá học của kim loại


Chia sẻ
Bình chọn:
4.3 bên trên 34 phiếu
Bài tiếp sau

Luyện bài Tập Trắc nghiệm Hóa lớp 9 - coi ngay
Báo lỗi - Góp ý
 |  |  |  |
 |  |  |  |
TẢI ứng dụng ĐỂ coi OFFLINE


Bài giải đang rất được quan tâm
× Báo lỗi góp ý
Vấn đề em chạm chán phải là gì ?
Sai chủ yếu tả
Giải cực nhọc hiểu
Giải không nên
Lỗi khác
Hãy viết cụ thể giúp Loigiaihay.com
gửi góp ý Hủy vứt
× Báo lỗi
Cảm ơn chúng ta đã sử dụng Loigiaihay.com. Đội ngũ giáo viên cần nâng cao điều gì để các bạn cho bài viết này 5* vậy?
Vui lòng nhằm lại tin tức để ad rất có thể liên hệ với em nhé!
Họ với tên:
nhờ cất hộ Hủy bỏ
Liên hệ chế độ






Đăng ký kết để nhận giải thuật hay và tài liệu miễn phí
Cho phép loigiaihay.com nhờ cất hộ các thông báo đến các bạn để nhận được các giải thuật hay cũng giống như tài liệu miễn phí.
Dãy hoạt động hóa học của kim loại lớp 9 có không ít tính chất không giống nhau và được thu xếp theo thứ tự sút dần của mức độ hoạt động. Bài viết dưới đây sẽ giúp đỡ bạn gồm thêm kiến thức có lợi về dãy hoạt dộng chất hóa học của kim loại lớp 9. Đồng thời, các bạn cũng có thể ứng dụng những lý thuyết để giải những bài tập có tương quan nhé!
1. đặc thù dãy hoạt động hóa học tập của sắt kẽm kim loại lớp 9
Kim một số loại khi được sắp xếp theo vật dụng tự giảm dần nhờ vào mức độ hoạt động là mức độ phản bội ứng với chất khác của chúng sẽ tạo nên thành dãy hoạt động hóa học tập của sắt kẽm kim loại như sau:

Bài thơ – Mẹo học tập thuộc dãy vận động hóa học tập của sắt kẽm kim loại lớp 9. Xem thêm: Cách Làm Chà Bông Thịt Bò - Ruốc Thịt Bò Cho Bé Ăn Dặm
3. Bài bác tập ứng dụng dãy hoạt dộng chất hóa học của kim loại lớp 9
Để có thể nắm được hết toàn bộ kiến thức, dưới đây là tổng hợp một số trong những bài tập áp dụng cơ phiên bản mà bạn cũng có thể tham khảo:
3.1 bài 1
Cho 20 gam lếu hợp bao gồm hai kim loại là Cu, Zn vào hỗn hợp axit H2SO4 loãng dư, tiếp đến thu được 4,48 lít khí (ở đktc). Yêu cầu:
a. Viết các phương trình phản ứng hóa học có thể xảy ra.
b. Xác định khối lượng chất rắn còn lại sau khi phản ứng.
Hướng dẫn giải bài xích tập:
Cu đứng sau H trong dãy vận động hóa học của sắt kẽm kim loại nên Cu không chức năng được cùng với axit H2SO4 loãng
a. Phương trình hóa học xảy ra là:
Zn + H2SO4 → Zn
SO4 + H2 (khí)
0,2 ß—————— 0,2 (mol)
b. Số mol của khí (H2) là: 4,48/22,4 = 0,2
=> khối lượng của kẽm là:m
Zn = 0,2 x 65 = 13 g.
=> cân nặng của đồng còn lại là: m
Cu = 21 – 13 = 8 gam
3.2 bài 2
Cho một vài phản ứng hóa học bên dưới đây, hiện nay tượng xẩy ra là gì? Viết gần như phương trình hóa học rất có thể xảy ra?
a. Mang đến dây kẽm nhúng vào dung dịch muối đồng sunfat:
Hiện tượng xảy ra: hỗn hợp muối có màu xanh lá cây nhạt dần, xuất hiện thêm chất rắn red color (Cu) bám vào mặt phẳng dây kẽm.Phương trình hóa học: CuCl2 (dd) + Zn (r) → Zn
Cl2 (dd) + Cu(r).
b. Thả thanh đồng vào dung dịch muối tệ bạc nitrat:
Hiện tượng xảy ra: hóa học rắn white color bạc lộ diện (Ag) bám vào bề mặt thanh đồng. Ag bị Cu xuất kho khỏi dung dịch muối, đề xuất dung dịch mong muốn dần gửi qua màu xanh da trời lam (muối Cu(NO3)2).Phương trình hóa học: Cu (r) + 2AgNO3 (dd) → Cu(NO3)2 (dd) + 2Ag ↓
c. Bỏ miếng nhôm vào dung dịch muối đồng clorua:
Hiện tượng xảy ra: mở ra chất rắn màu đỏ (Cu) dính vào mặt phẳng nhôm, màu hỗn hợp nhạt dần dần thành xanh nhạt.Phương trình hóa học: 2Al(r) + 3CuCl2 (dd) → 2Al
Cl3 (dd) + Cu(r)
d. Thả thanh kẽm vào dung dịch muối magie clorua
Không bao gồm hiện tượng xẩy ra do không có phản ứng hóa học giữa Zn và ý muốn Mg
Cl2
4. Kết luận
Bài viết trên đấy là những kiến thức về định hướng và bài bác tập áp dụng của dãy hoạt dộng chất hóa học của kim loại lớp 9 mà bạn cũng có thể tham khảo. Mong muốn những tin tức này sẽ có ích với các bạn và giúp cho bạn nhiều hơn nữa trong việc học tập nhé!
=>> các bạn hãy theo dõi loài kiến Guru để cập nhật bài giảng với kiến thức những môn học tập khác nhé!









